
La innovación biomédica y el compromiso de las compañías farmacéuticas con la investigación de nuevos medicamentos avanza de manera imparable a pesar de la pandemia. Como muestra el último informe anual sobre aprobaciones de tratamientos de la Agencia Europea de Medicamentos (EMA), 2021 registró el récord de nuevas moléculas autorizadas en los últimos 5 años en la región, con 54 principios activos, y sólo en este lustro la EMA ha dado luz verde a 200 sustancias completamente nuevas.
Oncología (con 12), vacunas y tratamientos contra la Covid-19 (7) y hematología y neurología (5) fueron las áreas terapéuticas con más aprobaciones el año pasado. Inmunología, reumatología, endocrinología, cardiovascular, metabolismo, dermatología, oftalmología, infecciosas, reproducción y gastroenterología han visto también aumentado su arsenal terapéutico.
Entre las 54 novedades sobresalen dos nuevos productos considerados terapias avanzadas. Asimismo, el informe de la EMA indica que se aprobaron 89 nuevas indicaciones para medicamentos ya autorizados, incluidas 35 para uso pediátrico.
Tiene especial relevancia que 19 de las 54 novedades terapéuticas (un 35%) hayan sido categorizadas como medicamentos huérfanos, lo que ratifica el impulso de la investigación por parte de la industria farmacéutica innovadora en al área de las enfermedades raras o poco frecuentes, una demanda constante entre profesionales sanitarios y pacientes y sus familiares.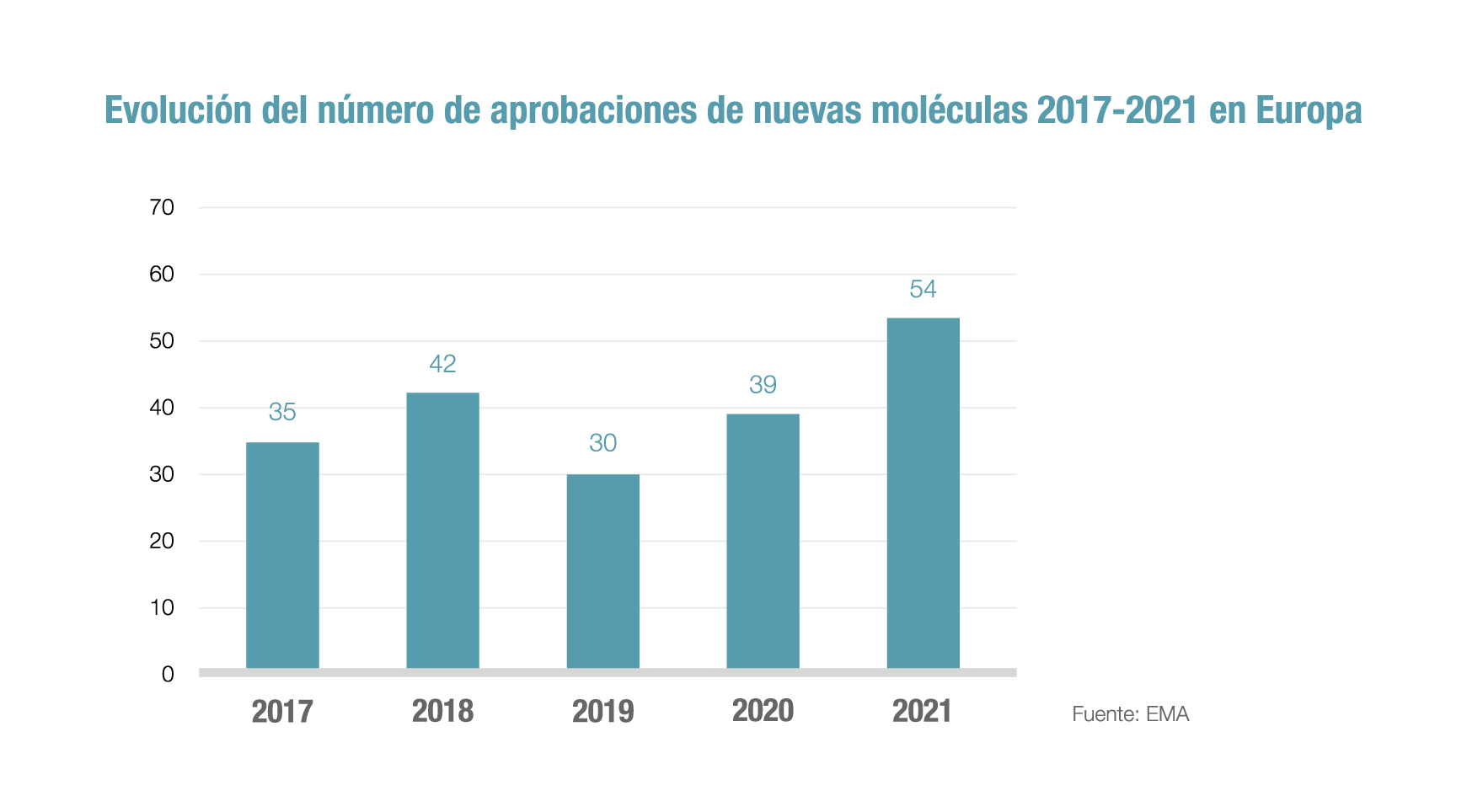 Resultados de cinco años del programa ‘Prime’
Resultados de cinco años del programa ‘Prime’
Asimismo, seis medicamentos obtuvieron el año pasado la designación Prime, que es el programa de la EMA que tiene como objetivo agilizar el acceso de los pacientes a medicamentos prometedores dirigidos a patologías con necesidades médicas no cubiertas mediante un procedimiento acelerado de evaluación para su posterior aprobación.
Como informaba la EMA a principios de mes, desde la puesta en marcha de Prime, en marzo de 2016, hasta el primer semestre de 2021 ha permitido la aprobación de 18 medicamentos. Entre ellos, 10 recibieron una autorización de comercialización condicional, que les permite acceder al mercado antes y llegar a los pacientes con mayor rapidez, y siete son fármacos de terapia avanzada, que tienen el potencial de remodelar el tratamiento de una amplia gama de afecciones. La mayor parte de estos fármacos (16) están indicados para enfermedades raras.
“El programa Prime ha tenido un impacto positivo en la autorización de nuevos medicamentos que abordan las necesidades médicas no cubiertas de los pacientes. El tiempo hasta la autorización de comercialización se redujo para los tratamientos que se beneficiaron del apoyo de Prime, dando a los pacientes un acceso más temprano a tratamientos transformadores que pueden marcar una diferencia real en su salud”, celebra la agencia europea.
EEUU: más de la mitad de nuevos medicamentos, ‘primeros de su clase’
El informe de la agencia reguladora estadounidense (FDA) arroja cifras similares de aprobaciones a las de la EMA. El Centro de Evaluación e Investigación del Medicamento de la citada FDA (CDER, por sus siglas en inglés) aprobó 50 nuevos tratamientos en 2021, una cifra ligeramente inferior a la de la EMA, lo que ocurre por primera vez en los últimos años.
Entre las novedades, el CDER identifica 27 fármacos (un 54%) como primeros de su clase (first-in-class), es decir, medicamentos que tienen mecanismos de acción diferentes a los de las terapias existentes o que tratan necesidades médicas no cubiertas. Y también que una de cada dos innovaciones es considerada como medicamento huérfano. “En 2021, se han aprobado muchas terapias diferentes, lo que va a ayudar a los pacientes a tener una mejor calidad de vida, reducir los síntomas de su enfermedad o gravedad y, en muchos casos, proteger a los pacientes contra enfermedades potencialmente mortales”, valora la agencia estadounidense.
En este sentido, la directora del Departamento de Acceso de Farmaindustria, Isabel Pineros, recuerda que “la innovación sólo importa si llega a los pacientes. Garantizar que los pacientes obtengan un acceso más rápido, equitativo y sostenible a medicamentos innovadores en Europa es un objetivo que compartimos las compañías farmacéuticas, los pacientes, las instituciones europeas y los gobiernos nacionales”.
“Contar con más y mejores tratamientos mejora y salva vidas -continúa Pineros-. Los medicamentos que se autorizaron el año pasado y los que están por venir son cada vez más complejos, más específicos. Por ello es necesario que este desarrollo científico, que está impulsando una nueva era en el campo de la investigación biofarmacéutica, vaya acompañado de un marco estable y de un procedimiento transparente de financiación y precio, que se articule a través de la colaboración entre autoridades sanitarias y compañías farmacéuticas. Ganar certidumbre en el proceso de financiación pública de los nuevos medicamentos es una necesidad de la industria farmacéutica, pero, sobre todo, de los pacientes”.
 | Innovamos para las personas
| Innovamos para las personas



