
De izquierda a derecha, Ángel Luis de la Cuerda, Humberto Arnés, Mª Ángeles Figuerola, Jesús Aguilar y Eladio González
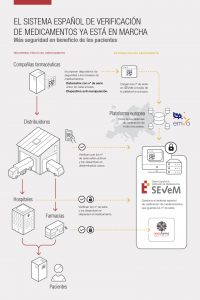
Prevenir la entrada de medicamentos falsificados en la cadena legal, reforzar la seguridad de los pacientes y cumplir con la normativa europea es el triple objetivo del Sistema Español de Verificación de Medicamentos (SEVeM), que, integrante de una plataforma europea, ya es una realidad en España tras su entrada en funcionamiento, el sábado 9 de febrero, al conectarse el conjunto de la cadena del medicamento, desde las compañías farmacéuticas fabricantes hasta las oficinas de farmacia de toda España, pasando por la distribución mayorista.
En virtud de este nuevo sistema, los medicamentos que estén sujetos a receta médica tienen que estar provistos de dos dispositivos de seguridad. El primero es un identificador único (en forma de código datamatrix) que contiene el código de producto, un número de serie de 20 caracteres generados por un algoritmo de aleatorización, el número de lote y la fecha de caducidad. De esta forma se puede verificar la autenticidad e identificar cada envase de medicamento de manera individual. Adicionalmente, en el caso de España, y a requerimiento de las autoridades nacionales, el código datamatrix contiene también el número nacional de reembolso, ya sea dentro del propio código de producto o en otro campo.
El segundo dispositivo de seguridad es un sistema antimanipulación para garantizar que el envase no ha sido abierto desde su salida de la cadena de producción hasta su dispensación en la oficina de farmacia.
A partir de ahora, y durante unos meses, hasta que se agoten los lotes liberados antes del 9 de febrero siguiendo el etiquetado antiguo, convivirán en las oficinas de farmacia los nuevos medicamentos serializados con los fármacos sin el identificador único. Ambos tipos mantendrán el cupón precinto.
La entrada en vigor del nuevo sistema y su conexión a escala europea se han llevado a cabo en tiempo y forma, y de modo satisfactorio para todas las partes pese a la complejidad del proceso, si bien su mayor éxito ha sido el trabajo conjunto y el consenso de los agentes que integran el nuevo sistema y su estrecha coordinación con las autoridades sanitarias. Así los explicaron los representantes del SEVeM, la Asociación Nacional Empresarial de la Industria Farmacéutica (Farmaindustria), la Asociación Española de Medicamentos Genéricos (AESEG), la Federación de Distribuidores Farmacéuticos (FEDIFAR) y el Consejo General de Colegios Oficiales de Farmacéuticos (CGCOF), en rueda de prensa celebrada este lunes en Madrid.
Un esfuerzo conjunto
Desde la industria farmacéutica innovadora, el director general de Farmaindustria y presidente del SEVeM, Humberto Arnés, explicó que para la industria “es absolutamente crítico evitar cualquier riesgo de falsificación de medicamentos, ya que la seguridad de los pacientes es lo más importante”. Arnés destacó el gran esfuerzo inversor que ha hecho la industria farmacéutica para adoptar la serialización, que demuestra una vez más –subrayó- que la industria farmacéutica “es un agente esencial del Sistema Nacional de Salud y está plenamente implicada en asegurar, y si es posible mejorar, la calidad de la prestación farmacéutica”.
 Según las estimaciones de Farmaindustria, las compañías farmacéuticas han incurrido en un coste global en las plantas españolas de unos 200 millones de euros derivado de la adaptación de las cadenas de producción a las exigencias de etiquetado del SEVeM. A esto hay que sumarle el coste derivado de la modificación de los procesos necesarios para la inclusión de los dispositivos de seguridad en los envases, actualizar la documentación de registro necesaria para las autorizaciones, y formalizar contratos con el repositorio europeo (EMVO) y el SEVeM, con el abono de las tasas correspondientes, para que pueda hacerse la carga y el mantenimiento de repositorios. La industria ha tenido además que revisar los contratos con sus proveedores y con terceras partes para ajustarlos a las actuaciones previstas en la nueva legislación de serialización.
Según las estimaciones de Farmaindustria, las compañías farmacéuticas han incurrido en un coste global en las plantas españolas de unos 200 millones de euros derivado de la adaptación de las cadenas de producción a las exigencias de etiquetado del SEVeM. A esto hay que sumarle el coste derivado de la modificación de los procesos necesarios para la inclusión de los dispositivos de seguridad en los envases, actualizar la documentación de registro necesaria para las autorizaciones, y formalizar contratos con el repositorio europeo (EMVO) y el SEVeM, con el abono de las tasas correspondientes, para que pueda hacerse la carga y el mantenimiento de repositorios. La industria ha tenido además que revisar los contratos con sus proveedores y con terceras partes para ajustarlos a las actuaciones previstas en la nueva legislación de serialización.
Ángel Luis Rodríguez de la Cuerda, secretario general de la Asociación Española de Medicamentos Genéricos (AESEG), reiteró que la incidencia de falsificación en España es mínima y siempre asociada a la compra de productos por internet. No obstante, como país miembro de la UE debemos incorporar esta directiva europea de obligado cumplimiento para incrementar la prevención de entrada de medicamentos falsificados. “A pesar del alto coste económico que hemos tenido que asumir en adecuación de cadenas de producción, implementación y mantenimiento del sistema de verificación, la industria farmacéutica del medicamento genérico también contribuye a incrementar, aún más, la seguridad para el paciente”, subrayó Rodríguez de la Cuerda.
Acceso al medicamento
El presidente de la Federación de Distribuidores Farmacéuticos (FEDIFAR), Eladio González Miñor, destacó que “el modelo de distribución farmacéutica español siempre ha garantizado el acceso de los ciudadanos a todos los medicamentos que necesitan en condiciones de equidad, calidad y seguridad, un último aspecto que con la puesta en marcha de SEVeM se verá reforzado”. Igualmente, resaltó el “compromiso de las empresas de distribución farmacéutica de gama completa con la seguridad del paciente y el esfuerzo realizado por los almacenes mayoristas para llevar a cabo las adaptaciones necesarias de cara a cumplir con los procedimientos que la normativa europea en materia de Antifalsificación les exige”. Según González Miñor, “la distribución ha cumplido con los plazos establecidos y todos los almacenes de las empresas asociadas en FEDIFAR verifican y desactivan los códigos de los medicamentos en los casos establecidos por la normativa”.
Por último, el presidente del Consejo General de Colegios Oficiales de Farmacéuticos (CGCOF), Jesús Aguilar, destacó que la profesión farmacéutica ha vuelto a demostrar, una vez más, su capacidad tecnológica y su compromiso con la seguridad de los pacientes. “Llevamos más de tres años de trabajo y podemos decir con orgullo que hemos cumplido en tiempo y forma con las exigencias de la normativa europea”, señaló Jesús Aguilar, quien añadió: “Las más de 22.000 farmacias que hay en España han estado preparadas y listas para arrancar el sistema de verificación de medicamentos, uno de los proyectos tecnológicos de mayor envergadura acometidos en el sector farmacéutico. Y la respuesta de los farmacéuticos ha sido ejemplar. Una respuesta que consolida nuestra posición de referente a nivel internacional”.
Iniciativa en toda Europa
El origen a este modelo de serialización de medicamentos se remonta a 2008, cuando la Comisión Europea presentó una propuesta legislativa para evitar la entrada de medicamentos falsificados en la cadena legal de suministro de medicamentos. Las autoridades europeas respondían así a una preocupación global ante la amenaza que para la salud pública representa la falsificación de medicamentos, un problema que afortunadamente en España, a día de hoy, tiene un carácter testimonial.
 Fruto de esta preocupación se adoptó, en 2011, la llamada Directiva antifalsificación, introduciendo una serie de medidas para prevenir esta lacra en el ámbito europeo. Posteriormente, en octubre de 2015 la Comisión adoptó el Reglamento Delegado correspondiente, que se publicó en febrero del año siguiente y que sería de aplicación tres años después de su publicación, el 9 de febrero de 2019. El nuevo modelo está estructurado como sistema de extremo a extremo, donde los distintos agentes de la cadena legal de suministro de medicamentos tienen asignadas sus correspondientes obligaciones.
Fruto de esta preocupación se adoptó, en 2011, la llamada Directiva antifalsificación, introduciendo una serie de medidas para prevenir esta lacra en el ámbito europeo. Posteriormente, en octubre de 2015 la Comisión adoptó el Reglamento Delegado correspondiente, que se publicó en febrero del año siguiente y que sería de aplicación tres años después de su publicación, el 9 de febrero de 2019. El nuevo modelo está estructurado como sistema de extremo a extremo, donde los distintos agentes de la cadena legal de suministro de medicamentos tienen asignadas sus correspondientes obligaciones.
Así, mientras que los fabricantes deben incluir en el embalaje exterior de los medicamentos el código datamatrix y el dispositivo antimanipulación, los distribuidores mayoristas pueden practicar verificaciones voluntarias en cualquier momento y además están obligados a verificar los medicamentos con mayor riesgo de falsificación, de modo que si eventualmente fueran falsificados no pasen inadvertidos, y por último las oficinas o servicios de farmacia u otros agentes autorizados para dispensar medicamentos deben verificar y desactivar el identificador único del envase que vayan a dispensar al paciente.
Un proceso complejo
Los socios de SEVeM (AESEG, Farmaindustria, FEDIFAR y CGCOF), que representan a los agentes de la cadena de distribución de medicamentos en España, constituyeron la entidad en el mes de julio de 2016. Desde entonces, SEVeM ha tenido que cumplir con distintos hitos, como la incorporación de su equipo técnico, la selección del proveedor tecnológico que ha desarrollado el sistema, la implantación de la infraestructura en España (que quedó conectada a la plataforma europea en el primer semestre del año pasado) o la integración de NodoFarma Verificación para hacer realidad la conexión de 22.000 farmacias españolas en un plazo de tiempo realmente breve.
“Gracias a la implicación de todos los agentes ha sido posible que el pasado 9 de febrero España cumpliera con los plazos impuestos por la legislación europea. Una semana antes ya estaban cargadas en el sistema más de 10.000 referencias de medicamentos, y alrededor del 50% de los almacenes de medicamentos ubicados en nuestro país estaban conectados. En tan solo cinco días, más de 8.000 farmacias se conectaron al sistema y, coincidiendo con el 9 de febrero, la práctica totalidad de las farmacias estaban ya verificando y desactivando los códigos de los medicamentos serializados”, explicó la directora general del SEVeM, Mª Ángeles Figuerola.
La responsable del SEVeM destacó, asimismo, que este nuevo sistema constituye “el primer paso en la digitalización y trazabilidad completa de la cadena del medicamento”, un proceso que beneficiará en primer lugar al paciente.
Identificador único
Aunque la vigencia de la verificación es ya una realidad, los nuevos envases dotados de identificador único coexistirán en los próximos meses en el mercado de manera legal con todavía gran cantidad de envases no serializados. Por lo tanto, al principio solo un número limitado de envases podrán ser verificados, ya sea porque no incorporan un identificador único o porque llevan datamatrix anteriores al 9 de febrero que no están adaptados completamente a las nuevas disposiciones. Sin embargo, los responsables del SEVeM esperan que en menos de un año el 98% de los envases que circulen en la cadena de suministro ya lleven un identificador único que pueda verificarse.
Más adelante, cuando todos los medicamentos que son financiados por el Sistema Nacional de Salud que circulen por el canal estén serializados, se podrá eliminar el actual cupón precinto, que dejará de ser necesario como comprobante de la dispensación. Entonces la desactivación de los números de serie se convertirá en la única prueba fehaciente para el reembolso por el Sistema Nacional de Salud del precio de los medicamentos dispensados a su cargo.
A juicio de Figuerola, “todo esto aportará eficiencia en diversos puntos de la cadena, por ejemplo, para los fabricantes, que ya no tendrán que troquelar los embalajes; para los farmacéuticos, que dejarán de recortar y pegar el cupón, o para las autoridades, que de manera automatizada podrán comprobar las dispensaciones”.
De cara al futuro, el SEVeM abrirá la puerta a otros desarrollos muy positivos para el Sistema Nacional de Salud en general y el paciente en particular, ya que el propio Reglamento europeo que lo regula prevé también que los Estados miembros puedan usar el sistema para otras finalidades todavía pendientes de definir en España y relacionadas con la farmacovigilancia, el reembolso y la farmacoepidemiología.
 | Innovamos para las personas
| Innovamos para las personas


